21世紀經濟報道記者 閆碩
8月28日,國家醫保局正式公布通過2025年醫保及商保創新藥目錄調整初步形式審查藥品名單。
與8月12日公布的版本相比,6個藥品形式審查結果發生變化,其中注射用利培酮微球、注射用雙羥萘酸曲普瑞林調整為不通過;左旋多巴注射液、葡萄糖酸鈣氯化鈉注射液調整為通過;另外,熊去氧膽酸口服混懸液仍為通過,但“通過申報條件”有所調整。
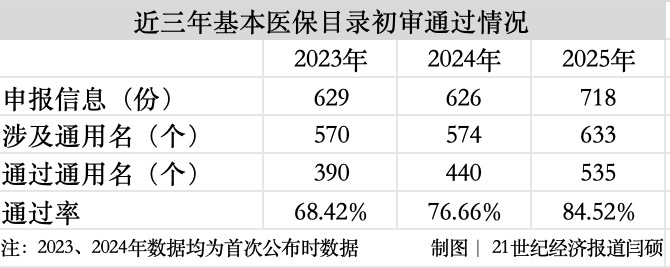
最終,2025年目錄調整申報階段國家醫保局共收到基本醫保目錄申報信息718份,涉及藥品通用名633個,535個通過形式審查,其中目錄外311個、目錄內224個。
梳理近幾年的形式審查情況可以發現,今年無論是通過數量還是通過率均有所增加。其中,2023年和2024年涉及藥品通用名變化不大,但通過率有顯著提升;今年涉及通用名大幅增加,超600個,通過率也已達到84.52%。這為更多藥品納入基本醫保目錄奠定了前提。
商保創新藥目錄首次出現,并與基本醫保目錄同步申報,最終申報信息141份,涉及藥品通用名141個,121個通過形式審查,其中同時申報基本醫保目錄和商保創新藥目錄的有79個。
兩份目錄中有諸多藥品值得關注。
6個藥品發生變化
2025年8月12日至8月18日,國家醫保局公示了初審通過藥品名單。公示期間,共收到75條反饋意見。隨后,國家醫保局進行了復核和修正,共6個藥品發生變化,均為申報基本醫保目錄的藥品。
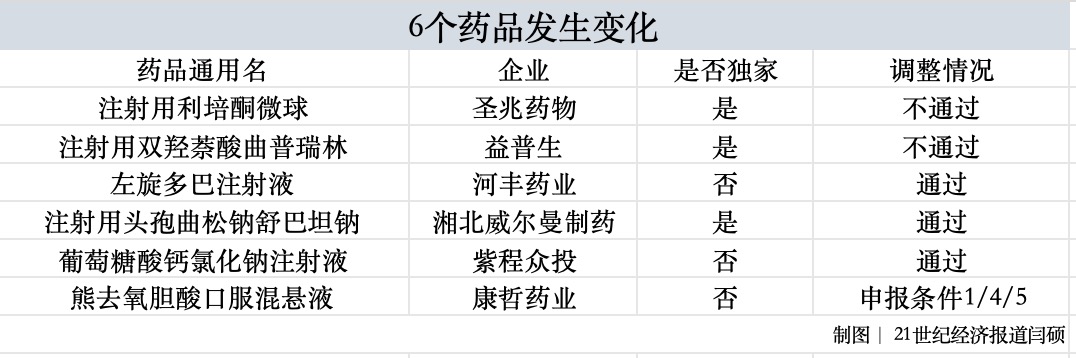
其中,注射用利培酮微球改為不通過形式審查。該產品為圣兆藥物的獨家品種,2025年2月首次在中國大陸上市,用于治療精神類疾病。同疾病治療領域,綠葉制藥集團的瑞欣妥?(注射用利培酮微球(Ⅱ))于2021年進入醫保。
另一款產品注射用雙羥萘酸曲普瑞林也調整為不通過形式審查。該產品為益普生的獨家品種,于2023年在中國大陸上市,主要用于治療前列腺癌、性早熟等。同疾病治療領域產品包括亮丙瑞林,原研一月劑型于1996年在我國獲批,三月劑型于2000年獲批,已被納入醫保乙類常規目錄。
此次通過初審的左旋多巴注射液為河豐藥業的產品,并非獨家品種,主要用于帕金森病(原發性震顫麻痹),腦炎或合并有腦動脈硬化以及中樞系統的一氧化碳與錳中毒后的癥狀性帕金森綜合征(非藥源性震顫麻痹綜合征);也用于急性肝功能衰竭引起的肝昏迷。
目前,同疾病治療領域產品較多,包括多巴絲肼、左旋多巴等進入醫保甲類目錄的品種,也包括卡比多巴、屈昔多巴等多個進入醫保乙類目錄的品種。相比于口服多巴胺能制劑,左旋多巴注射液在特殊患者覆蓋、生物利用度、起效速度等方面均有明顯優勢。
另一個調整通過的注射用頭孢曲松鈉舒巴坦鈉為湘北威爾曼制藥的獨家品種,2016年首次在中國大陸上市,用于治療由對頭孢曲松單藥耐藥、對本復方敏感的產β-內酰胺酶細菌引起的中、重度感染。同藥理作用的藥品以頭孢哌酮/舒巴坦、頭孢噻肟/他唑巴坦為主。相較而言,注射用頭孢曲松鈉舒巴坦鈉的抗菌譜更廣、安全性更高,且是目前唯一長效復方抗生素。
紫程眾投的非獨家品種葡萄糖酸鈣氯化鈉注射液也通過了初審,主要用于急性低鈣血癥、鎂中毒、氟中毒。整體來看,葡萄糖酸鈣注射液在我國的上市時間為1981年,2009年納入國家基本醫療目錄,屬于醫保甲類。相比于其他品種,紫程眾投的產品臨床應用方便、便捷,且安全性更高。
此外,康哲藥業的非獨家產品熊去氧膽酸口服混懸液通過形式審查,審查結果改為符合目錄外申報條件1/4/5,相比之前的1/4,增加了“5”的罕見病范疇。
多款創新藥引發關注
梳理基本醫保目錄和商保創新藥目錄可以發現,兩份目錄均以新藥為主,其中,基本醫保目錄中滿足條件1或2的達到303個,商保創新藥目錄滿足條件1的達111個。
其中“條件1”為2020年1月1日至2025年6月30日(下同)期間獲批上市的新通用名藥品,“條件2”則為期間適應癥或功能主治發生重大變化的藥品。
另外,基本醫保目錄中近250個藥品為獨家品種,商保創新藥目錄中的121個均為獨家品種。
多款產品備受市場關注。比如多次沖擊醫保均失敗的“百萬抗癌藥”CAR-T產品,今年合源生物的納基奧侖賽注射液、馴鹿生物的伊基奧侖賽注射液、科濟藥業的澤沃基奧侖賽注射液押注醫保、商保“雙目錄”。
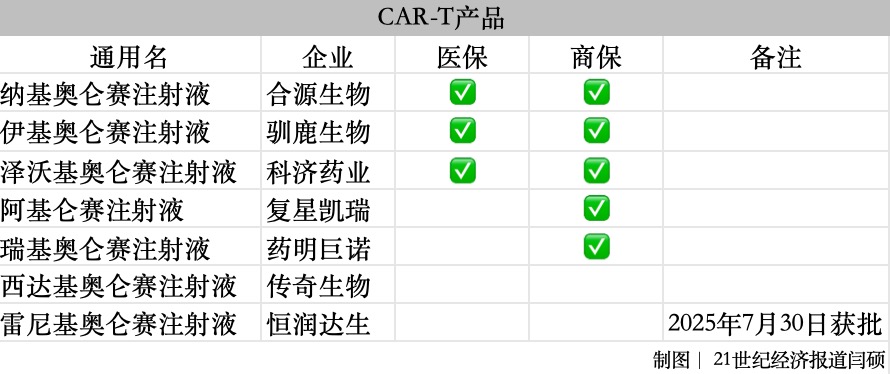
復星凱瑞的阿基侖賽注射液此前四次沖擊醫保,藥明巨諾的瑞基奧侖賽注射液此前三次沖擊醫保,均以失敗告終,今年則通過了商保創新藥目錄。
另外,傳奇生物的西達基奧侖賽注射液和恒潤達生的雷尼基奧侖賽注射液未出現在初審名單,后者獲批時間為今年7月30日,不在目錄申報窗口期內。
對于該類品種的最終“命運”,上海市衛生和健康發展研究中心主任金春林此前向21世紀經濟報道記者表示,由于今年多了商保創新藥目錄的渠道,所以在基本醫保目錄中的3款產品,如果沒有降低至30萬元以內,很難有突破。
兩份目錄中也同時出現了多個“全球首個且唯一”的產品。比如全球首個且唯一的AKT抑制劑卡匹色替片、注射用戈沙妥珠單抗。
卡匹色替片為阿斯利康的獨家產品,于今年4月首次在中國大陸上市,主要用于治療局部晚期或轉移性乳腺癌,填補了CDK4/6i耐藥后精準靶向治療的臨床空白。
注射用戈沙妥珠單抗為吉利德的獨家產品,于2022年6月在中國大陸上市,用于治療乳腺癌患者,是目前在HR+/HER2-晚期乳腺癌唯一獲得PFS/OS雙重顯著獲益的Trop-2 ADC,目錄內和市場上均暫無同一治療領域和同作用機制的ADC(抗體偶聯藥物)藥品。
此外,多款PD-1/L1備受關注,比如基本醫保目錄中神州細胞的獨家產品菲諾利單抗注射液,商保創新藥目錄中的恒瑞醫藥的阿得貝利單抗注射液、羅氏的阿替利珠單抗注射液、輝瑞的舒格利單抗注射液等多款產品。也不難發現,其中不乏跨國藥企的身影。
罕見病用藥或迎曙光
在藥品申報時,“條件5”為罕見病藥品目錄所收錄的藥品,基本醫保目錄中以該條件申報的有37個,商保創新藥目錄中則為35個,其中兩份目錄均通過的達到19個。
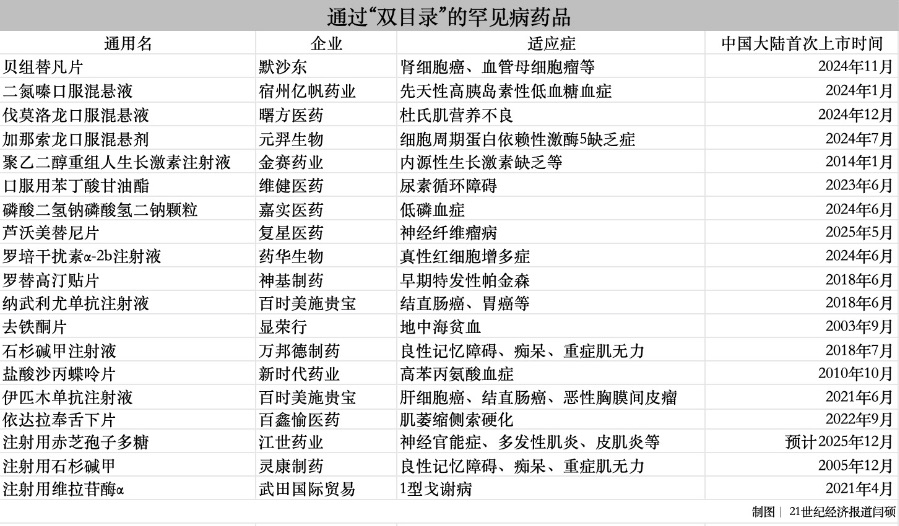
在這19個產品中包括百時美施貴寶的2款產品,分別為納武利尤單抗注射液、伊匹木單抗注射液。納武利尤單抗是全球首個獲批的PD-1抑制劑,聯合伊匹木單抗是我國目前唯一獲批的雙免方案(簡稱O+Y),近年來多次沖擊醫保,但尚未有實質性進展。
業內觀點認為,此次同時通過兩份目錄初審,無疑為“O+Y”后續的市場推廣與患者可及性注入一劑“強心針”。
此外,有2款產品適應癥基本一致:萬邦德制藥的石杉堿甲注射液和靈康制藥的注射用石杉堿甲,主要用于重癥肌無力。
目前,與石杉堿甲注射液屬于同治療領域和同藥理作用藥品,且屬于注射液劑型的,醫保目錄中有兩種,加蘭他敏和新斯的明注射劑,三者均具有膽堿酯酶抑制作用。石杉堿甲相較加蘭他敏,對乙酰膽堿酯酶的選擇性更好、安全性更高。
特別值得一提的是,此次申報的產品基本條件為2020年1月1日至2025年6月30日期間獲批,但江世藥業的注射用赤芝孢子多糖預計2025年12月獲批上市卻通過了初審。據介紹,該產品為全國獨家赤芝孢子多糖凍干產品,凍干產品極其嚴格地控制了含水量,解決了多糖水溶液易氧化和易水解難題,保證了產品的有效成分不降解,減少了雜質的生成。確保了產品的有效性和安全性。
另外,結合凍干產品降低了多糖在水溶液中的聚合作用,減少了由于多糖聚合而引起的大分量物質的增加,升級了質控標準,在質量標準中增加了分子量分布的質控方法,確保了患者的用藥安全。
在罕見病領域,近段時間一家企業引起廣泛關注。今年以來,在創新藥引領醫藥板塊大漲的情形下,罕見病藥企北海康城撕開一道“裂縫”,今年1月2日至今漲幅已超1500%,截至8月28日收盤,每股2.21港元。其旗下3款創新藥物均通過商保創新藥目錄初審,分別為注射用維拉苷酶β、氯馬昔巴特口服溶液、艾度硫酸酯酶β注射液。
此次目錄調整初審階段已過,8~9月為專家評審階段;9~10月為談判/競價/價格協商階段;10~11月則為最終的公布結果階段。創新藥、罕見病等領域最終將取得哪些突破,值得期待。

















